
Van Pols tot Praktijk: Advies voor huisartsen over het beoordelen van AF-meldingen via smartwatches.
Slimme zogenaamde “smart-watches” horloges worden steeds vaker ingezet om atriumfibrillatie (AF) vroegtijdig op te sporen. [...]
Als huisarts en als cardioloog zien we regelmatig volwassen patiënten met een verdikte hartspier of linker ventrikelhypertrofie.
2 veel voorkomende oorzaken zijn: een verhoogde bloeddruk of een aortaklepstenose. Hierbij treedt een adaptieve reactie van het hart op een chronisch verhoogde workload. Ook andere vormen van een "belasting” op de hartspier kunnen een wandverdikking geven zoals extreem sporten/ sporthart en ernstig overgewicht.
En bepaalde medicamenten zoals anabole steroiden, hydrochloroquine en tacrolimus kunnen een oorzaak zijn.
Bij hypertensie is het hebben van LVH een marker voor eindorgaan schade en een sterke voorspeller van congestief hartfalen, coronaire hartziekten en beroertes. Het risico op dergelijke cardiovasculaire events neemt toe met toenemende linkerventrikelmassa (LVM). LVH is een reversibele risicofactor; de regressie ervan als reactie op behandeling met antihypertensiva verbetert de CV-uitkomst en de prognose op lange termijn aanzienlijk.
Hypertrofe Cardiomyopathie
Bij een wanddikte van de linker ventrikel van ≥ 15mm die niet alleen wordt verklaard door workload op het hart, spreken we van hypertrofische cardiomyopathie (HCM). HCM is de meest voorkomende erfelijke hartaandoening op de volwassen leeftijd met 1:500.
Mutaties in sarcomeereiwitten (de contractiele eiwitten van de hartspiercel) kunnen dit ziektebeeld veroorzaken. Het meest frequent (75-80%) betreft het mutaties in MYH7 dat codeert for beta myosin heavy chain en MYBPC3 dat codeert voor myosin binding protein C.
Bij HCM is er een verstoorde organisatie van de cardiomyocyten, er ontstaat fibrose en microvasculaire ziekte. De LV hypertrofie is progressief, mn in het septum, gedurende adolescentie tot middelbare leeftijd.
Patiënten met HCM hebben een hogere mortaliteit in vergelijking met de algemene bevolking. Het ziektebeeld kent een zeer variabel verloop variërend van asymptomatische patiënten tot ernstig hartfalen. Er is een verhoogd risico op atriumfibrilleren en beroerte. Ook al is er in het algemeen een lage kans op plotse hartdood < 1% per jaar, plotse dood op jonge leeftijd kan een eerste manifestatie van de ziekte zijn.
Differentiaal diagnose
Genetische en niet-genetische aandoeningen waarbij LVH ontstaat kunnen zich presenteren met een mindere mate van wandverdikking; in deze gevallen vereist de diagnose van HCM evaluatie van andere kenmerken, waaronder voorgeschiedenis, familiegeschiedenis, niet-cardiale symptomen en tekenen, afwijkingen van het elektrocardiogram (ECG), laboratoriumtests en (multimodale) cardiale beeldvorming.
In de differentiaaldiagnose van LVH ontdekt op de volwassen leeftijd spelen, in 5-10% van de casus, zeldzame aandoeningen zoals amyloidose, Anderson-Fabry, maar ook mitochondriale en neuromusculaire ziekten die zich vaker al op de kinderleeftijd manifesteren. Hier zal in deze nieuwsbrief niet nader op in worden gegaan.
Hoe kun je onderscheid te maken tussen LVH door toegenomen workload en LVH obv een erfelijke cardiomyopathie (HCM)? En bij wie is het nu een goed idee om DNA diagnostiek in te zetten naar een erfelijke oorzaak?
De volgende factoren zijn belang in de initiële afweging:
Ook is het in de interpretatie van de LV massa en wanddikte rekening te houden met:
Het beeld is meer passend bij LVH op basis van hypertensie wanneer er sprake is van concentrische LVH en wanneer het ECG normaal is. Ook kunnen we afname van de LV hypertrofie zien in de 6-12 maanden wanneer hypertensie adequaat behandeld wordt.
En bij aanvullende beeldvorming: andere tekenen van langdurige hypertensie zoals aortadilatatie. Bij MRI wordt (vrijwel) geen fibrose gezien.
Kijkend naar aanwijzingen die meer wijzen op een onderliggende erfelijke hypertrofe cardiomyopathie. Vaker zien we een sterk afwijkend ECG met, behoudens toegenomen voltages, repolarisatiestoornissen die zich ook naar de anterior of inferior afleidingen uitbreiden, ook zien we soms pathologische Q golven en geleidingsstoornissen.
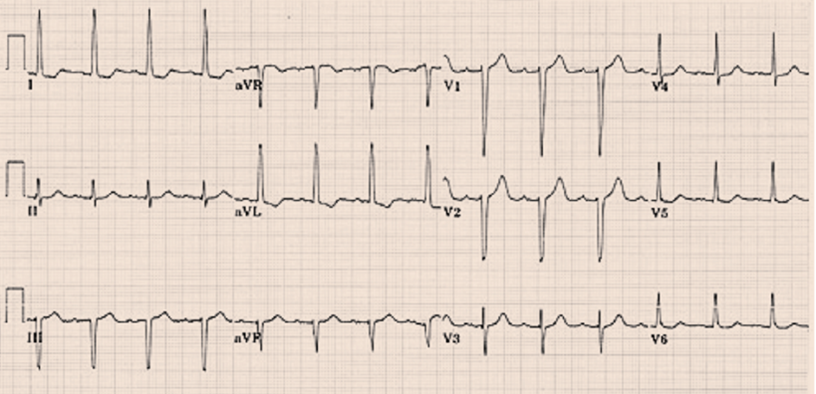
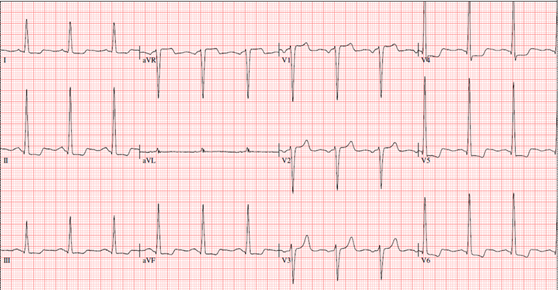
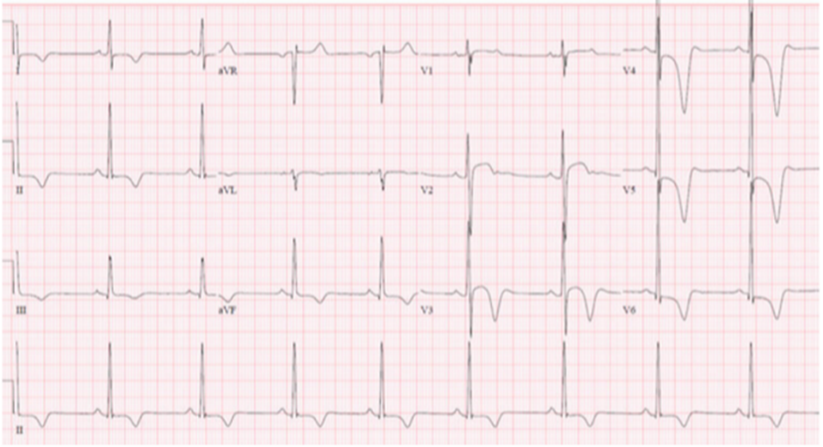
Aanwijzingen bij cardiale beeldvorming die meer passen bij een erfelijke HCM:
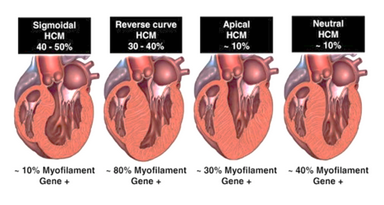
De opbrengst van DNA onderzoek bij een hypertroof hart is variabel, gemiddeld rond 40%, maar is veel hoger in reversed curve HCM namelijk rond 80%.
The Mayo HCM Genotype Predictor score (Mayo Score) geeft een pre-test waarschijnlijkheid op een positieve genetische test. Hoe hoger de score hoe waarschijnlijker het is dat een pathogene mutatie gevonden wordt bij DNA diagnostiek.

Bij een verdenking op een erfelijke hypertrofe cardiomyopathie kunt u de patiënt verwijzen naar onze polikliniek voor erfelijke hartziekten, hiervoor kan de patiënt terecht in 5 van onze vestigingen: HartKliniek Almere, HartKliniek Bilthoven, HartKliniek Oisterwijk, HartKliniek Rijswijk en HartKliniek Vlaardingen.
Een volledige anamnese en familie-anamnese wordt afgenomen. En in kaart brengen van het cardiale beeld met ECG, echocardiogram en eventueel Holter ECG. Er vindt een duidelijke uitleg plaats over het (erfelijke) ziektebeeld. Op indicatie wordt een MRI van het hart aangevraagd. Ook zal worden vastgesteld of er een indicatie voor DNA diagnostiek is. Zo ja dan wordt dit in gang gezet. Hieruit volgen weer familieadviezen die duidelijk besproken zullen worden. We werken samen met de afdeling Klinische Genetica van zowel Amsterdam UMC als het UMC Utrecht.
Referentie
Heeft u inhoudelijke vragen aangaande het onderwerp van deze nieuwsbrief? Stuurt u dan gerust een email naar communicatie@hartkliniek.com.

Slimme zogenaamde “smart-watches” horloges worden steeds vaker ingezet om atriumfibrillatie (AF) vroegtijdig op te sporen. [...]

Hypertensieve aandoeningen tijdens zwangerschap komen voor bij ongeveer 10% van de gevallen, waarbij pre-eclampsie optreedt bij 3–4% [...]

Digitalis werd jarenlang gezien als ouderwetse cardiologie, maar nieuwe data zetten het middel opnieuw in de schijnwerpers. [...]